
本研究团队在METTL3的亚细胞定位筛查中发现,不同于大多数情况METTL3与METTL14、WTAP共定位于细胞核(三者组成甲基转移酶复合体MTase,负责催化m6A修饰的产生),在胃癌、前列腺癌、胰腺癌、白血病中,METTL3特异性富集在肿瘤细胞的细胞质中。并且METTL3在细胞质的富集程度与肿瘤进展密切相关,其中以胃癌最为显著(图1)。后续的功能实验证实,胞质特异性表达在的METTL3确实能够促进胃癌的发生发展。
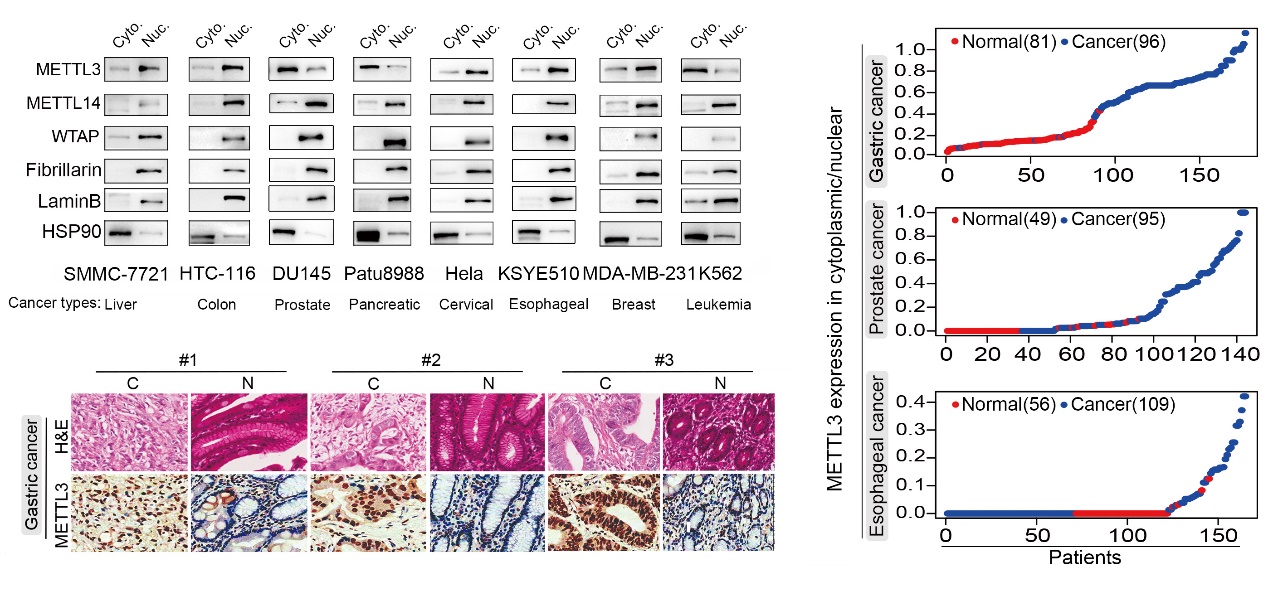
图1. METTL3在胃癌细胞质中特异性富集
本研究团队进一步通过MeRIP-seq、CLIP-seq探究METTL3在胃癌细胞质中的致癌新机制。分析和验证发现,胃癌细胞中METTL3更倾向于结合在非m6A修饰的转录本上并增强其翻译效率,提示其不依赖于m6A修饰的新型功能(图2)。进而通过质谱分析鉴定出一系列在细胞质中与METTL3互作的蛋白质。与以往报道的在细胞核内作为m6A“书写器”或细胞质内作为m6A“阅读器”的身份所不同的是,我们在胃癌中发现,METTL3能够与细胞质中poly(A)结合蛋白PABPC1相互作用,通过增强PABPC1与帽结合复合物eIF4F结合的稳定性促进mRNA 成环,并最终影响翻译起始和核糖体再循环过程(图3)。此外,野生型和甲基化转移酶活性缺失的METTL3均能通过促进非m6A修饰的表观遗传调控因子的的翻译加速胃癌进展;相反,在胃癌细胞系和患者来源的异种移植瘤模型中抑制METTL3的表达均能延缓胃癌细胞的生长,提示METTL3在胃癌中的潜在治疗价值。
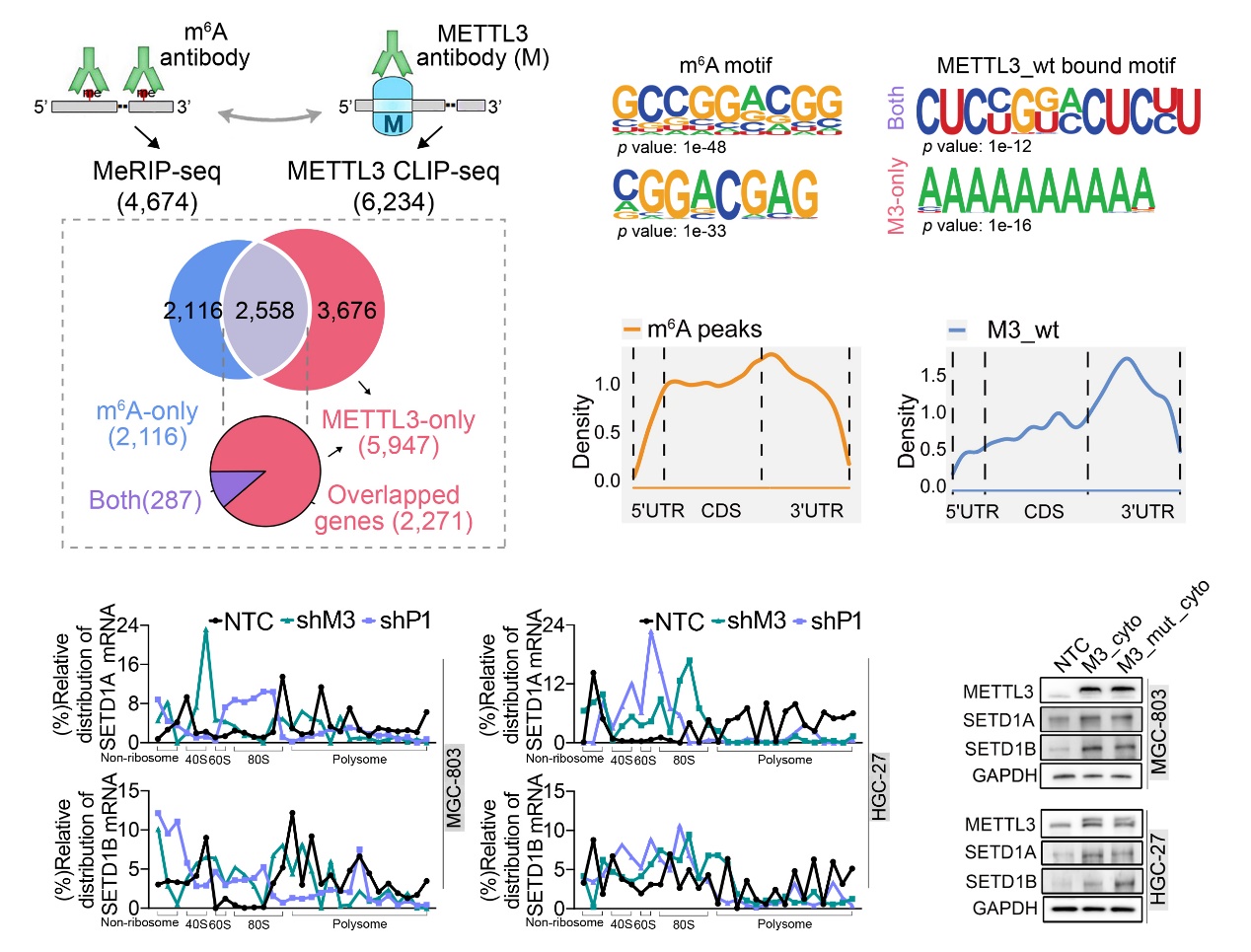
图2. METTL3倾向结合于非m6A修饰的转录本并促进其翻译
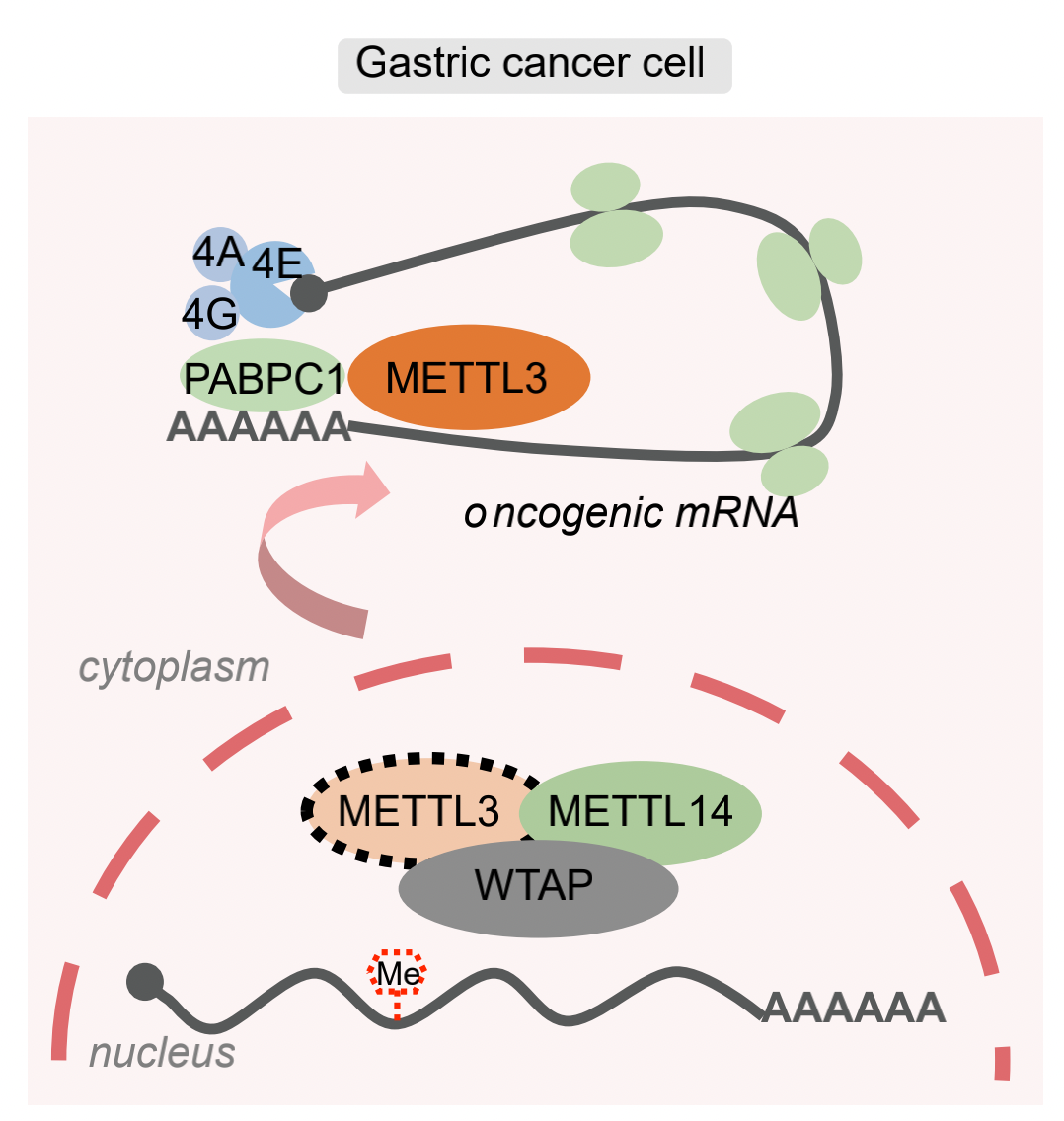
图3. METTL3通过与PABPC1互作调控关键表观因子的翻译促进胃癌发生发展
本研究揭示了METTL3不依赖于m6A的新型、非经典调控机制,丰富了对RNA甲基化关键分子METTL3的全面认识;更重要的是,我们发现在包括胃癌在内的多种肿瘤中,细胞质中的METTL3丰度与患者生存期密切相关。因此,在这些肿瘤中,抑制METTL3或METTL3-PABPC1互作代表了比靶向其甲基转移酶活性更有前途的治疗方法。
本研究工作得到中国医学科学院医学与健康科技创新工程(2021-I2M-1-019;2021-I2M-1-040)等项目的资助。基础医学研究所余佳教授和王芳教授、药物研究所金晶教授、重庆肿瘤医院的邹冬玲教授为论文共同通讯作者,基础医学研究所魏雪菊、霍悦博士、皮静楠博士、高玉风博士、何漫漫博士、南方医科大学饶栓教授为论文的共同第一作者。
论文链接:https://www.nature.com/articles/s41556-022-00968-y